肺がんの治療法執筆者:聖路加国際病院院長 福井 次矢
肺がんとは、どんな病気でしょうか?
おもな症状と経過
肺がんの初期はとくに症状はなく、発生する場所にもよりますが、実際に症状が出てくるのはかなり進行してからのこともあります。肺のどの場所に発生したかで、症状やその後の経過は異なりますので、発生した場所によって肺がんを分類する方法が一般的に用いられます。
肺の入口付近にできるものを中心型肺がん(肺門部肺がん)、肺の奥のほうにできるものを末梢型肺がん(肺野部肺がん)といいます。中心型肺がんでは、比較的早い時期から、せき、痰、血痰の三大症状が現れます。かぜに似ていますが、鼻汁や頭痛、のどの痛みなどはありません。レントゲンでは見つけにくく、喀痰細胞診という痰の検査をすると、早期に見つけることができます。一方、末梢型肺がんは早期には症状がありませんが、レントゲン検査で比較的見つけやすいタイプです。
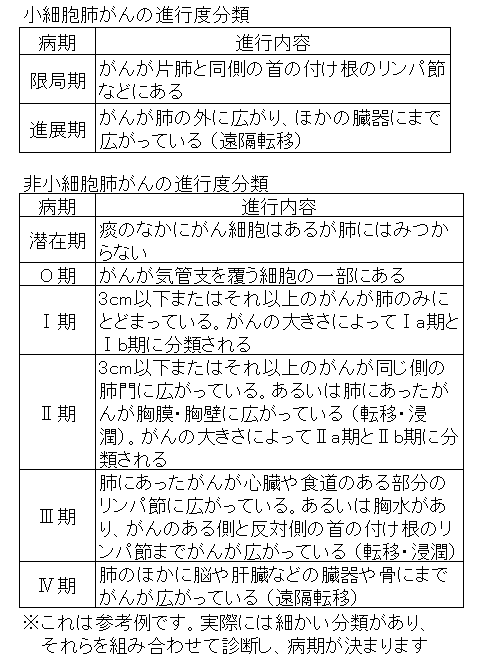
また、組織型といってがん細胞の種類による分類方法もあり、小細胞肺がんと非小細胞肺がんの二つに分類され、このうち非小細胞肺がんは腺がん、扁平上皮がん、大細胞がんに分類されます。このほか、進行の度合いによっても分類されます。一般に小細胞肺がんは進行が速く、手術ができない進行がんの状態で発見されることが多いため、予後があまりよくありません。
非小細胞肺がんは、肺がん全体の82~90パーセントを占め、その内訳は腺がん約50パーセント、扁平上皮がん約35パーセント、大細胞がん約6パーセントとなっています。治療方針はそれぞれのがんの種類によって異なります。
小細胞肺がんの病期は限局型、進展型の二つに大きく分けられ、がんが脳や骨など体のほかの臓器に転移するのは進展型になります。非小細胞肺がんでは、脳やほかの臓器への転移は進行末期のIV期になります。
病気の原因や症状がおこってくるしくみ
最大の原因はたばこで、1日の喫煙本数が多いほど、また喫煙年数が長いほど、肺がんになる確率が高くなります。それ以外では、大気汚染、ちりやほこりなどの刺激を長年受けていると肺がんになりやすいといわれています。
病気の特徴
比較的お年寄りに多く発病します。現在、日本人の死因の第1位はがんですが、そのなかでも肺がんはもっとも多くなっています。病気にかかった人の数は胃がんのほうが多いにもかかわらず、肺がんによる死亡が多いのは、それだけ治療困難な病気であることを示しています。
治療法とケアの科学的根拠を比べる
| 治療とケア | 評価 | 評価のポイント | |
|---|---|---|---|
| 予防として禁煙を励行する | ★5 | 喫煙は肺がんの原因の一つで、喫煙しない人と比べて10~30倍肺がんになりやすく、禁煙すると、喫煙している人と比べて肺がんになる危険性が20パーセントから90パーセント減少します。禁煙した期間で減少率は異なり、15年間以上禁煙した場合、喫煙者に比べて肺がんになる危険性が90パーセント減少すると報告されています。これらのことは、非常に信頼性の高い臨床研究によって確認されています。 根拠(1)~(3) | |
| 小細胞肺がん | 化学療法と放射線療法を併用する | ★5 | 小細胞肺がんは診断がついた時点で片方の肺だけに見つかることはなく、全身のいろいろな部分に転移していることが多いので通常外科治療を行うことは少なく、行うとしても単独では行いません。化学療法、放射線療法を組み合わせた治療を行います。化学療法によって約80パーセント以上が治療に反応しますが、再発率が高く、生存率は限局期では診断されてから14カ月から20カ月、進展期では8カ月から13カ月です。限局期の治療において、化学療法と放射線療法を併用した場合は、しない場合に比べて約15パーセント死亡を減少させることが、非常に信頼性の高い臨床研究によって確認されています。 根拠(4) |
| 非小細胞肺がん | 早期発見、早期切除を基本に、病期(病気の進み具合)に応じた治療をする | ★5 | I期の治療は手術が基本になります。肺がん全体の5年生存率は10~13パーセントですが、I期では全体で75パーセント、Ia期で82パーセント、Ib期で68パーセントと比較的良好です。II期も手術が基本になりますが、I期より5年生存率は低く、30~45パーセントと報告されています。III期で手術ができない患者さんのうち、状態がよい患者さんの場合には、放射線療法と化学療法を併用したほうが、放射線療法のみの場合よりも生存率がよくなると報告されています。IV期では、患者さんの状態がよい場合は、全身化学療法を行った場合、最良の緩和ケア(がんを治すのではなく患者さんの苦痛を取り除くためのケア)だけを行った場合に比べて、平均1.5カ月生存期間が延びたと報告されています。これらのことは、非常に信頼性の高い臨床研究によって確認されています。 根拠(5)~(8) |
| がん性胸膜炎には、胸水吸引後、癒着療法を行う | ★4 | 全肺がんの7~15パーセントの患者さんで経過中に悪性胸水(がん性胸膜炎の別称で、がん細胞が胸腔内にばらまいたように発生し、胸水を生じたもの)を認めます。組織型のなかでは腺がんがもっとも多いといわれています。呼吸困難がある場合には、胸水を抜きとったあとに癒着療法を行います。癒着療法は、胸水の原因となっているがんのまわりにより強い炎症をおこして癒着させ、胸水がたまる腔をなくしてしまうもので、胸腔に強い炎症をおこさせる化学物質を注入します。癒着療法の成功率は約70パーセントといわれ、副作用として痛みが平均23パーセント、発熱が平均19パーセントにおこると報告されています。こうしたことは、信頼性の高い臨床研究によって確認されています。 根拠(9) | |
| 脳転移には放射線療法を行う | ★4 | 肺がんは脳転移の頻度が高いがんです。とくに小細胞肺がんは症状があまりなく、脳に転移した状態で発見されることも多いため、患者さんの全身状態や年齢、症状を考慮し、放射線療法を行います。全脳照射が一般的で、生存率を伸ばす効果が信頼性の高い臨床研究によって示されています。 根拠(10) | |
| 骨転移には、放射線療法を行う | ★4 | 約90パーセントに効果を認め、そのうちの約半数では十分に痛みをコントロールできたことが信頼性の高い臨床研究によって報告されています。 根拠(11) | |
| がん化学療法に伴う好中球減少症にはG-CSF製剤を用いる | ★4 | G-CSF製剤の使用によりがん化学療法の副作用でおこる好中球減少症(白血球の一種である好中球が減少し、感染症を合併しやすくなる)による発熱は68パーセントから38パーセントへ減少したと報告されています。このことは信頼性の高い臨床研究によって確認されています。ただし死亡率を減らす効果は認められませんでした。アメリカ臨床がん学会では、慎重に使用するよう勧めています。 根拠(12)(13) | |
| 抗がん薬使用時、とくにプラチナ製剤使用時にはあらかじめ制吐薬を用いる | ★5 | がん化学療法に伴う嘔吐に対しては、副腎皮質ステロイド薬とプリンペラン(メトクロプラミド)の併用がもっともよいといわれています。非常に信頼性の高い臨床研究によると、使用しない場合は89パーセントの患者さんで嘔吐がありましたが、この2剤の併用療法で48パーセントに減らすことができたと報告されています。 根拠(14) | |
よく使われる薬の科学的根拠を比べる
抗がん薬
| 主に使われる薬 | 評価 | 評価のポイント | |
|---|---|---|---|
| ブリプラチン/ランダ(シスプラチン)+ラステット/ベプシド(エトポシド)またはトポテシン/カンプト(塩酸イリノテカン)またはナベルビン(酒石酸ビノレルビン) | ★5 | プラチナ製剤のシスプラチンに、エトポシド、塩酸イリノテカン、酒石酸ビノレルビンのいずれかを組み合わせた2剤併用療法の効果は、非常に信頼性の高い臨床研究で確認されています。 根拠(15)(16)(18) | |
| ユーエフティ(テガフール・ウラシル配合剤) | ★5 | 非小細胞肺がんの手術後、テガフール・ウラシル配合剤を用いた群と用いなかった群を比較したところ、用いたほうは5年生存率に差があったとの非常に信頼性の高い臨床研究があります。 根拠(17) | |
| タキソール(パクリタキセル) | ★5 | 非常に信頼性の高い臨床研究によって非小細胞肺がんに効果のあることが確認されています。 根拠(19) | |
| タキソテール(ドセタキセル水和物) | ★5 | 非小細胞肺がんのIII期またはIV期で、シスプラチンによる治療を行ったあとの患者さんに効果があったことが非常に信頼性の高い臨床研究で確認されています。 根拠(20) | |
| パラプラチン(カルボプラチン)+ラステット/カンプト(エトポシド) | ★5 | 非小細胞肺がんのIII期またはIV期で、カルボプラチンとエトポシドを併用した場合、緩和ケアのみの患者さんと比較して効果のあったことが非常に信頼性の高い臨床研究で確認されています。 根拠(21) | |
| ジェムザール(塩酸ゲムシタビン)+ブリプラチン/ランダ(シスプラチン) | ★5 | 塩酸ゲムシタビンは、シスプラチンと併用することで非小細胞肺がんのIII期またはIV期の患者さんに効果のあることが非常に信頼性の高い臨床研究で確認されています。 根拠(22) | |
がん性胸膜炎
| 主に使われる薬 | 評価 | 評価のポイント | |
|---|---|---|---|
| 癒着療法に用いる薬 | ピシバニール(OK-432) | ★5 | OK-432は非常に信頼性の高い臨床研究によって効果が確認されています。 根拠(23) |
G-CSF製剤
| 主に使われる薬 | 評価 | 評価のポイント | |
|---|---|---|---|
| ノイトロジン〔レノグラスチム(G-CSF)〕 | ★4 | レノグラスチム(G-CSF)は信頼性の高い臨床研究によって効果が確認されています。 根拠(12)(13) | |
制吐薬
総合的に見て現在もっとも確かな治療法
がん細胞のタイプにより治療法が異なる
肺がんは、どのような細胞のタイプなのかにより、治療方法が大きく異なります。小細胞肺がんであって、胸腔内に限局した小さい腫瘍については放射線療法と抗がん薬を組み合わせた治療を、胸腔内にかなり広がっている場合は全身にがん細胞が広がっている可能性が高く、抗がん薬を用います。
非小細胞肺がんでは、比較的限局している場合には手術を、そうでない場合には放射線療法や抗がん薬を組み合わせるか、またはそれぞれを単独に用いるのが一般的です。
副作用の吐き気を抑える効果的な薬剤がある
抗がん薬に伴う吐き気・嘔吐については、あらかじめ副腎皮質ステロイド薬やプリンペラン(メトクロプラミド)、カイトリル(塩酸グラニセトロン)などを用いることで、かなり抑制することができます。
病態に応じた治療法がある
がんが広がったり、転移したりすることでさまざまな合併症がおきてきますので、それぞれの治療を行います。
肺がんの浸潤によるがん性胸膜炎には胸水を吸引した後、起炎薬のピシバニール(OK-432)を使用し、癒着療法を行います。脳転移あるいは骨転移には放射線療法、がん化学療法に伴う好中球減少症にはG-CSF製剤のノイトロジン(レノグラスチム)の使用など、それぞれの病態に有効な治療法が確立されています。
しかし、あくまでもなにもしない場合やそのほかの治療法に比べて一時的に症状を軽減できる可能性が高いことをいっているにすぎず、残念ながら、多くの患者さんでは、完全に治癒することは望めないのが現状です。
抗がん薬の再評価が進められている
近年、抗がん薬の有効性を、その副作用との兼ね合いで本当に使う価値があるかどうか、検証しようとする臨床研究が多く行われつつあります。それらの結果によっては新たな治療法が開発されたり、従来ある治療法が比較されたりして、標準的な治療法はこれから短期間のうちに変わる可能性が高いと思われます。
おすすめの記事
根拠(参考文献)
- (1) Samet JM, Wiggins CL, Humble CG, et al. Cigarette smoking and lung cancer in New Mexico. Am Rev Respir Dis. 1988;137:1110-1113.
- (2) Peto R, Darby S, Deo H, et al. Smoking, smoking cessation, and lung cancer in the UK since 1950: combination of national statistics with two case-control studies. BMJ. 2000;321:323-329.
- (3) The Health Benefits of Smoking Cessation: A Report of the Surgeon General. US Dept of Health and Human Services, Washington, 1990.
- (4) Pignon JP, Arriagada R, Ihde DC, et al. A meta-analysis of thoracic radiotherapy for small-cell lung cancer. N Engl J Med. 1992;327:1618-1624.
- (5) Martini N, Bains MS, Burt ME, et al. Incidence of local recurrence and second primary tumors in resected stage I lung cancer. J Thorac Cardiovasc Surg. 1995;109:120-129.
- (6) Mountain CF. A new international staging system for lung cancer. Chest. 1986;89:225S-233S.
- (7) Marino P, Preatoni A, Cantoni A. Randomized trials of radiotherapy alone versus combined chemotherapy and radiotherapy in stages IIIa and IIIb nonsmall cell lung cancer. A meta-analysis. Cancer. 1995;76:593-601.
- (8) Non-small Cell Lung Cancer Collaborative Group. Chemotherapy in non-small cell lung cancer: a meta-analysis using updated individual patient data from 52 randomised clinical trials. Br Med J. 1995;311:899-909.
- (9) Walker-Renard PB, Vaughan LM, Sahn SA. Chemical pleurodesis for malignant pleural effusions. Ann Intern Med. 1994;120:56-64.
- (10) Chang DB, Yang PC, Luh KT, et al. Late survival of non-small cell lung cancer patients with brain metastases. Influence of treatment. Chest. 1992;101:1293-1297.
- (11) Hoegler D. Radiotherapy for palliation of symptoms in incurable cancer. Curr Probl Cancer. 1997;21:129-183.
- (12) Messori A, Trippoli S, Tendi E. G-CSF for the prophylaxis of neutropenic fever in patients with small cell lung cancer receiving myelosuppressive antineoplastic chemotherapy: meta-analysis and pharmacoeconomic evaluation.J Clin Pharm Ther. 1996;21:57-63.
- (13) Ozer H, Armitage JO, Bennett CL, et al. American Society of Clinical Oncology. 2000 update of recommendations for the use of hematopoietic colony-stimulating factors: evidence-based, clinical practice guidelines. American Society of Clinical Oncology Growth Factors Expert Panel. J Clin Oncol. 2000;18:3558-3385.
- (14) Kris MG, Gralla RJ, Tyson LB, et al. Controlling delayed vomiting: double-blind, randomized trial comparing placebo, dexamethasone alone, and metoclopramide plus dexamethasone in patients receiving cisplatin. J Clin Oncol. 1989;7:108-114.
- (15) Pujol JL, Carestia L, Daures JP. Is there a case for cisplatin in the treatment of small-cell lung cancer? A meta-analysis of randomized trials of a cisplatin-containing regimen versus a regimen without this alkylating agent. Br J Cancer. 2000;83:8-15.
- (16) Noda K, Nishiwaki Y, Kawahara M, et al. Japan Clinical Oncology Group. Irinotecan plus cisplatin compared with etoposide plus cisplatin for extensive small-cell lung cancer. N Engl J Med. 2002;346:85-91.
- (17) Wada H, Hitomi S, Teramatsu T. Adjuvant chemotherapy after complete resection in non-small-cell lung cancer. West Japan Study Group for Lung Cancer Surgery. J Clin Oncol. 1996;14:1048-1054.
- (18) Greco FA, Gray JR Jr, Thompson DS, et al. Vinorelbine plus cisplatin versus cisplatin plus vindesine and mitomycin C in stage IIIB-IV non-small cell lung carcinoma: a prospective randomized study. Lung Cancer. 2002;37:179-187.
- (19) Socinski MA. Single-agent paclitaxel in the treatment of advanced non-small cell lung cancer. Oncologist. 1999;4:408-416.
- (20) Shepherd FA, Dancey J, Ramlau R, et al. Prospective randomized trial of docetaxel versus best supportive care in patients with non-small-cell lung cancer previously treated with platinum-based chemotherapy. J Clin Oncol. 2000;18:2095-2103.
- (21) Helsing M, Bergman B, Thaning L, et al. Quality of life and survival in patients with advanced non-small cell lung cancer receiving supportive care plus chemotherapy with carboplatin and etoposide or supportive care only. A multicentre randomised phase III trial. Joint Lung Cancer Study Group. Eur J Cancer. 1998;34:1036-1044.
- (22) Evans WK, Kocha W, Gagliardi A, et al. The use of gemcitabine in non-small-cell lung cancer. Provincial Lung Cancer Disease Site Group. Provincial Systemic Treatment Disease Site Group. Cancer Prev Control. 1999;3:84-94.
- (23) Luh KT, Yang PC, Kuo SH, et al. Comparison of OK-432 and mitomycin C pleurodesis for malignant pleural effusion caused by lung cancer. A randomized trial. Cancer. 1992;69:674-679.
- (24) Matsui K, Fukuoka M, Takada M, et al. Randomised trial for the prevention of delayed emesis in patients receiving high-dose cisplatin. Br J Cancer. 1996;73:217-221.
- 出典:EBM 正しい治療がわかる本 2003年10月26日初版発行